Archiv Detail
Resistenzen schmuggeln sich durch Kläranlagen
12. Dezember 2018 |
Mehr als 95 Prozent aller Bakterien, die aus menschlichen Fäkalien ins Abwasser gelangen, werden in Abwasserreinigungsanlagen entfernt. Trotzdem sind im Auslauf noch viele antibiotikaresistente Bakterien anzutreffen. Wie lässt sich das erklären? Der Mikrobiologe Helmut Bürgmann und seine Gruppe wollten es wissen und untersuchten in zwölf Abwasserreinigungsanlagen (ARA), was mit resistenten Bakterien im Verlauf des Reinigungsprozesses geschieht. Zudem interessierte es die Forschenden, ob Stressoren im Abwasser – zum Beispiel Antibiotika, Biozide oder Schwermetalle – das Auftreten von Resistenzgenen beeinflussen.
Ein «harter Kern» von hartnäckigen Resistenzen
In den zwölf ARAs haben die Forschenden Biomasseproben aus dem Zufluss, den biologischen Reinigungsstufen sowie dem Ablauf entnommen. Daraus extrahierten sie DNA, sequenzierten diese und identifizierten diejenigen Genabschnitte, die für Resistenzen gegen Antibiotika codieren. Zwar haben die Forschenden generell deutlich weniger resistente Bakterien im gereinigten Abwasser nachgewiesen als im Zulauf. Aber: «Der relative Anteil der resistenten Mikroorganismen nimmt in der ARA zu», sagt Bürgmann.
Die Forschenden fanden viele unterschiedliche Resistenzgene, deren Zusammensetzung innerhalb der ARA stark variierte. Eine kleine Gruppe von Resistenzgenen kam auf allen Stufen der Reinigung vor. Dieser «harte Kern» schmuggelt sich durch die ARA und ist vergleichsweise häufig anzutreffen. Aber rund 70 Prozent der verschiedenen Resistenzgene, die mit dem Abwasser in die ARA gelangen, werden im Verlauf des Reinigungsprozesses eliminiert. Dafür kommen aber auch neue hinzu: «Rund 40 Prozent der Resistenzen im Auslauf der ARA haben ihren Ursprung vermutlich im Belebtschlamm», sagt Bürgmann.
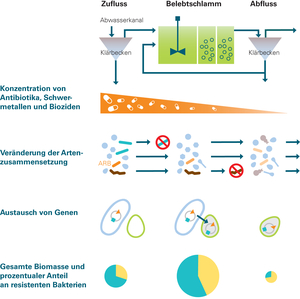
Die Grafik zeigt mögliche Prozesse, welche die Zusammensetzung und Häufigkeit von Antibiotikaresistenzgenen auf dem Weg durch eine ARA beeinflussen. Die Gesamtmenge an Bakterien ist in der biologischen Reinigungsstufe am höchsten und ist im Ausfluss deutlich geringer als im Zufluss. Aber: Der Anteil an resistenten Bakterien nimmt zu (gelbe Fläche im Kuchendiagramm), Resistenzen werden also angereichert.
(Grafik: Liz Amman, Quelle: Bürgmann et al., 2018)
Überleben dank Resistenz
Die Forschenden vermuten, dass die Bedingungen in der ARA einen Überlebensvorteil für resistente Mikroorganismen bieten. Ein Hinweis dafür sei, dass sich zwischen der Häufigkeit von Resistenzen und dem Vorkommen von manchen Antibiotika ein Zusammenhang zeigte – obwohl diese in der ARA nur in sehr tiefen Konzentrationen vorhanden sind. Zudem waren die Resistenzgene in der ganzen ARA bis zum Ablauf tatsächlich aktiv. Dass Belebtschlammbakterien häufig Resistenzen tragen, führt Bürgmann auch auf das enge Beieinander der Mikroorganismen in der ARA zurück: «Die Bakterien in den biologischen Reinigungsstufen enthalten zum Teil Resistenzgene, die zu 100 Prozent identisch sind mit denen von Krankheitserregern. Diese haben sie vermutlich durch Genaustausch erworben.»
Mobile Gene
Nebst den eigentlichen Resistenzgenen suchten Bürgmann und seine Gruppe deshalb auch nach sogenannten Mobilitätsgenen. Diese sind ein Hinweis darauf, dass Teile der Erbsubstanz zwischen verschiedenen Bakterien ausgetauscht werden. Wie sich zeigte, befanden sich diese Gene häufig in enger Nachbarschaft zu Resistenzgenen. Das weist darauf hin, dass zwischen menschlichen Krankheitserregern und anderen Bakterien ein substantieller Austausch von Resistenzgenen stattfindet. Das hat Folgen: «Wenn Resistenzen auf Belebtschlammbakterien übertragen werden und diese in die Umwelt gelangen, können sie dort vermutlich besser überleben als die Krankheitserreger», gibt Bürgmann zu Bedenken. Die einfachste Methode um dies zu verhindern sei, die Biomasse in der ARA möglichst vollständig aus dem Wasser zu eliminieren. Die neuen Reinigungsstufen zur Elimination von Mikroverunreinigungen, die Schweizer Kläranlagen in den nächsten Jahren erhalten, werden dazu einen Beitrag leisten.