News
Eawag-Test mit Fischzellen ersetzt Tierversuche
24. Juni 2021 |
In Produkten des Alltags, in der Landwirtschaft oder der Industrie kommen eine Vielzahl von Chemikalien zum Einsatz. Viele davon gelangen irgendwann auch in die Umwelt. Damit diese Stoffe für den Markt zugelassen werden dürfen, müssen die Hersteller vorab beweisen können, dass sie für Mensch und Natur unbedenklich sind. Dies geschieht mit Toxizitätstests, bei denen Lebewesen der Wirkung der Chemikalien ausgesetzt werden. Dabei sterben jedes Jahr Tausende Fische, weil an ihnen die Wirkung auf aquatische Wirbeltiere getestet wird.
Dank einem vom Wasserforschungsinstitut Eawag in den letzten Jahren entwickelten Testverfahren dürfte dies bald Vergangenheit sein. Dieser Test, der auf isolierten Kiemenzellen der Regenbogenforelle beruht, wurde jetzt von der Organisation für wirtschaftliche Zusammenarbeit und Entwicklung (OECD) als neueste Leitlinie im Bereich der Umwelttoxikologie freigegeben. Damit ist der Weg bereitet für tierversuchsfreie Zulassungsverfahren.
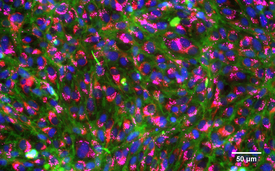
Angefärbte, gesunde Kiemenzellen von Regenbogenforellen: Zellkerne (blau), Membranen (grün), Mitochondrien (rot), Lysosome (pink).
(Foto: Vivian Lu Tan, Eawag)
Grosses Interesse der Wirtschaft
Bei dem sogenannten Fischzelllinientest handelt es sich um die weltweit erste Alternative zu Versuchen mit lebenden Fischen. Die neue OECD-Richtlinie ermöglicht es Unternehmen, den Fischzelllinientest für die Produktentwicklung und als Teil der Dossiers für die Chemikalienzulassung einzusetzen. «Es besteht seitens der Industrie ein grosses Interesse an tierversuchsfreien Tests», bestätigt Prof. Kristin Schirmer, Abteilungsleiterin an der Eawag, die zusammen mit Melanie Fischer (ebenfalls Eawag) diese Pionierarbeit federführend vorangetrieben hat. Denn einerseits wachsen die Ansprüche an die Umweltrisikobewertung, andererseits steigt die Anzahl neuer Chemikalien und Produkte, die getestet werden müssen, stetig. Darüber hinaus schont der Fischzelllinientest auch Ressourcen: Die Miniaturisierung durch den Einsatz der Zellen erlaubt, Chemikalien, Wasser und Zeit einzusparen.
«Es besteht seitens der Industrie ein grosses Interesse an tierversuchsfreien Tests.»
Kristin Schirmer
Kristin Schirmer geht davon aus, dass auch die Zulassungsbehörden, so etwa die ECHA in Helsinki oder die US EPA in den USA, den Fischzelllinientest zunehmend als gleichwertigen Ersatz zum regulären Fischtest akzeptieren werden: «Die OECD-Empfehlung war der letzte wichtige Schritt von unserer Seite, nachdem unsere Methode vor zwei Jahren bereits von der ISO zertifiziert wurde. Damit dürfte einem tierversuchsfreien Zulassungsverfahren nichts mehr im Wege stehen».
Damit trägt die Eawag dazu bei, die Toxikologie weiterzuentwickeln und leistet einen wesentlichen Beitrag zur Reduktion von Tierversuchen. Denn für ökotoxikologische Tests wurden im Jahr 2019 allein in der Schweiz Versuche an knapp 8000 Fischen durchgeführt.
Der Fischzelllinientest kurz erklärt
Die erste Idee
Dies setzt den Schlusspunkt unter eine lange und intensive Zeit, die Beharrlichkeit und ein unterstützendes Umfeld erforderte. Die Idee zu diesem Testverfahren hatte Schirmer bereits während ihrer Doktorarbeit Mitte der 1990er-Jahre: An der University of Waterloo (CAN) arbeitete sie damals mit exakt der gleichen Zelllinie, auf der die Methode heute noch beruht. Die Zelllinie geht zurück auf Schirmers Doktorvater Niels C. Bols, der die Zellen aus den Kiemen der Regenbogenforelle erstmals isolierte und so kultivierte, dass man sie beliebig oft vermehren kann.
«Wir haben deshalb Kiemenzellen gewählt, da es die Kiemen sind, die durch ihre grosse Oberfläche im Fisch als erstes mit einer Chemikalie in Kontakt kommen» erklärt Schirmer. Schädigt die Chemikalie die Kiemenzellen, bedeutet das für den Fisch, dass lebenswichtige Funktionen, wie etwa die Sauerstoffzufuhr, nicht mehr funktionieren. «Indem wir also beobachten, wie die Kiemenzellen durch eine Chemikalie geschädigt werden, können wir vorhersagen, wie sich diese Chemikalie auf einen lebenden Fisch auswirken würde» so Schirmer.
Die Bewährungsprobe
Der Zuschlag für einen Projektvorschlag, den Schirmer im Jahr 2006 vom Europäischen Rat der Chemischen Industrie (CEFIC) erhielt, markierte den eigentlichen Startschuss für die Entwicklung des nun validierten Fischzelllinientests. Schirmer setzte ihre Forschung zunächst als Abteilungsleiterin am Leipziger Helmholtz-Zentrum für Umweltforschung fort und ab 2008 als Abteilungsleiterin an der Eawag. Im Jahr 2009 stiess die Ingenieurin und Laborantin Melanie Fischer zum Team.
«In einem ersten Schritt entwickelten und optimierten wir unsere Methode und verglichen die Ergebnisse mit den regulären Tests an Fischen», sagt Schirmer. Eine 2013 publizierte Studie konnte so erstmals belegen, dass der neue Fischzelllinientest für über 30 Chemikalien zu den gleichen Toxizitätswerten gelangt wie der Fischtest. «Danach mussten wir aufzeigen, dass die Methode auch in anderen Laboratorien funktioniert», sagt Schirmer. An der dazu durchgeführten internationalen Ringstudie in den Jahren 2013-2014 nahmen sechs Labore aus Industrie und Hochschulen teil. Ihre Ergebnisse, die sie mit der Eawag-Methode erzielten, erwiesen sich als wiederholbar und vergleichbar.
Am Ziel
Diese Studiendaten legten den Grundstein für die ISO-Zertifizierung 2019 und die OECD-Richtlinie 2021. «Die Zertifizierung durch international abgestützte Organisationen ist sehr wichtig, da sich nur so sicherstellen lässt, dass die Tests weltweit standardisiert durchgeführt und somit die Ergebnisse auch anerkannt werden», sagt Schirmer. Von der Einreichung bei der OECD bis zur jetzt erfolgten Validierung verstrich eine rekordkurze Zeit von nur zwei Jahren, in der die Methode noch einmal in einem aufwändigen Prozess überarbeitet wurde, um die Vorschläge und Meinungen von Experten aus vielen verschiedenen Vertreterländern und Organisationen zu harmonisieren. Unterstützt wurde das Team dabei von den Ländervertretern der Schweiz (Petra Kunz, Bundesamt für Umwelt BAFU) und Norwegen (Sjur Andersen, norwegisches Umweltbundesamt und Adam Lillicrap, NIVA). Eszter Simon (ebenfalls BAFU) hat die Arbeiten als Expertin unterstützt.
«In der raschen Verabschiedung dieser ersten In-vitro-Methode für Ökotoxizitätstests spiegelt sich das Engagement der OECD-Länder für die Reduktion von Tierversuchen.»
Leon van der Wal, OECD
Dass die Richtlinie in so kurzer Zeit verabschiedet werden konnte, führt Schirmer auf das Interesse und die grosse Unterstützung aller Beteiligten zurück: «Es war eine aktive Diskussion mit den OECD-Ländern, mit der Industrie, NGOs und den Zulassungsbehörden.» Das bestätigt auch Leon van der Wal von der OECD: «In der raschen Verabschiedung dieser ersten In-vitro-Methode für Ökotoxizitätstests spiegelt sich das Engagement der OECD-Länder für die Reduktion von Tierversuchen. Zudem ist das auf die gut organisierte und transparente Art und Weise zurückzuführen, in der die federführenden Länder kommuniziert haben, sowie auf die harte Arbeit der Methodenentwickler und der OECD-Experten, die diese Methode überprüft haben.»
Kristin Schirmer stellt zurückblickend fest: «Unsere Lernkurve war sehr steil. Aber die Investition von Zeit und Energie hat sich gelohnt: Dieser Erfolg für tierversuchsfreie Alternativen in der Ökotoxikologie ist grossartig und etwas was bleibt.»
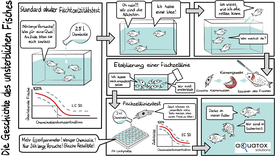
Die Entwicklung eines Fischzelllinientests zur Bestimmung von akuter Fischtoxizität.
(Bild: aQuaTox-Solutions)
Forschung mit Preis ausgezeichnet
Die Arbeit der Eawag für tierversuchsfreie Testmethoden ist von grosser Bedeutung. Das sieht auch das 3R Kompetenzzentrum Schweiz (3RCC) so: Der Verein möchte Tierversuche ersetzen, verringern und verbessern und verlieh Kristin Schirmer und Melanie Fischer 2019 den 3Rs Award für ihre Forschung. Zudem erhielten die Forscherinnen 2019 rund 251 000 Franken vom 3RCC zugesprochen. Damit arbeiten sie daran, dass für die Kultivierung der Zellen aktuell noch notwendige fötale Kälberserum durch ein serumfreies Medium zu ersetzen.
aQuaTox-Solutions
Aufgrund des wachsenden Interesses von Unternehmen, Kläranlagenbetreibern und Umweltämtern, den Test als Service in Anspruch zu nehmen, gründete sich im Jahr 2017 das Eawag-Spin-off aQuaTox-Solutions. Es ist weltweit der erste Anbieter für dieses und andere Fischzelllinien-basierte Testverfahren. Mit der Zertifizierung durch die OECD, und der damit einhergehenden Bestätigung der hohen Robustheit, Übertragbarkeit und Vergleichbarkeit, dürfte das Interesse an diesem Testverfahren weiter steigen
Titelbild: Eawag