Archiv Detail
Wie tot ist tot?
30. Oktober 2018 |
Die Zusammensetzung der menschlichen Darmflora hat einen grossen Einfluss auf das Immunsystem und die Nährstoffaufnahme. Zudem lässt sich bei vielen Darmkrankheiten beobachten, dass sich die Darmflora – im Fachjargon Darmmikrobiota genannt – im Verlauf der Krankheit verändert.
Daher wird derzeit intensiv erforscht, wie Mikroorganismen aus dem menschlichen Darm therapeutisch eingesetzt werden könnten – so auch am Institut für Lebensmittelwissenschaften, Ernährung und Gesundheit der ETH Zürich (IFNH). In ihrer vor kurzem publizierten Dissertation stellte die ETH-Doktorandin Lea Bircher die Konservierung von Darmbakterien ins Zentrum. Damit diese lebenden Mikroorganismen in der Medizin oder als Nahrungsergänzungsmittel verwendet werden können, dürfen sie bei der Aufbewahrung keinen Schaden nehmen. Bircher wählte sechs funktionell verschiedene Bakterienstämme aus und untersuchte, ob und wie gut diese drei Monate in tiefgefrorenem (-80°C) oder gefriergetrocknetem Zustand überstehen, wenn unterschiedliche Gefrierschutzmittel zugegeben werden.
Wissenstransfer im Bereich Labormethoden
Frederik Hammes, von der Eawag-Abteilung Umweltmikrobiologie unterstützte dieses Forschungsvorhaben mit seinem Know-how im Bereich der Durchflusszytometrie, einem Messverfahren, das unter anderem schnellere Analysen ermöglicht als das Heranziehen von bakteriellen Kolonien oder molekularbiologische Techniken.
«Völlig neu war die Durchflusszytometrie für uns nicht», sagt Clarissa Schwab. Sie hat die Doktorarbeit von Bircher am IFNH betreut. «Aber in unserem Labor wurde seit Jahren nicht mehr damit gearbeitet; deshalb waren wir froh, auf die Kenntnisse der Eawag zurückgreifen zu können.»
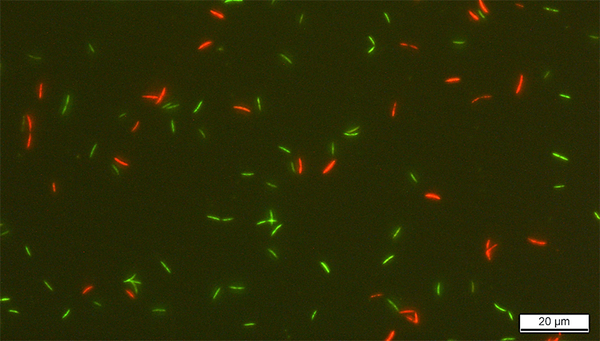
Frederik Hammes arbeitet bei der Analyse von Trink- und Abwasser schon sehr lange mit der Durchflusszytometrie und verfügt über grosse Erfahrung mit verschiedenen Methoden, um dabei die Lebensfähigkeit von Bakterien, die im Wasser enthalten sind, zu bestimmen. Gemeinsam erörterten Bircher und Hammes, welches dieser Verfahren sich am besten für die Beurteilung der Darmbakterien nach der Konservierung eignet. Sie entschieden sich relativ rasch für das Einfärben der Bakterien mit SYBR Green und Propidiumiodid (SGPI). Damit lässt sich erkennen, ob die Membran (Aussenhülle) von Bakterien beschädigt ist. Unbeschädigte Bakterien erscheinen im Durchflusszytometer (Messgerät) grün, bei beschädigter Membran weisen sie eine rote Färbung auf.
Der Grund für diese Wahl: Mit dem SGPI-Einfärbeverfahren ist die Eawag besonders gut vertraut – die Methode wurde von der Forschungsgruppe von Frederik Hammes für die Durchflusszytometrie optimiert und im Jahr 2016 standardisiert. Einige Probeläufe im Eawag-Labor zeigten, dass sich damit auch die von Bircher ausgewählten Darmbakterien gut untersuchen lassen. Nach einer Schulung an der Eawag führte die junge Forscherin ihre durchflusszytometrischen Analysen in den Labors der ETH eigenständig durch.
Gefrierschutzmittel haben positiven Effekt
Zur Beurteilung der Überlebensrate der Probiotika zog Bircher vor und nach der Konservierung Kulturen der verschiedenen Stämme heran. Die SGPI-Methode habe ihr wertvolle komplementäre Informationen zur Lebensfähigkeit der einzelnen Proben geliefert. Sie konnte in ihrer Arbeit zeigen, dass das Beifügen von Gefrierschutzmitteln wie Zucker, Inulin oder Glycerol die Überlebensrate der Bakterien teilweise deutlich erhöht. Die einzelnen Gefrierschutzmittel funktionieren jedoch nicht bei allen Bakterien und Konservierungsverfahren gleich gut.
Alle von Bircher untersuchten Bakterien gelten in Fachkreisen als spezielle Hoffnungsträger – man spricht dabei von «Probiotika der nächsten Generation». Doch bis diese tatsächlich auf den Markt gelangen, sind noch zahlreiche weitere Untersuchungen vonnöten.
Konferenz am Anfang
Der fachliche Austausch zwischen Clarissa Schwab und Frederik Hammes begann 2015 an einer Konferenz an der Eawag. Unter dem Titel «How Dead Is Dead» beleuchtete diese Veranstaltung die Grenzen des bakteriellen Lebens: Wann ist eine Bakterienzelle tot und wie lässt sich das messen? Zellen können sich in einem Ruhezustand befinden, in dem ihre metabolischen und physiologischen Prozesse soweit zurückgefahren sind, dass sie nicht mehr detektierbar sind. Können solche Zellen «wiederbelebt» werden? Diese Fragen sind wissenschaftlich noch nicht abschliessend beantwortet – weder in der Medizin noch in der Trinkwasser-Mikrobiologie.
Die Arbeiten von Lea Bircher wurden vom Schweizerischen Nationalfonds (Sinergia 35150) und der ETH Zürich unterstützt.
Publikationen
Foto
Darmbakterien Roseburia intestinalis eingefärbt mit SYBR Green und Propidiumiodid (SGPI). In Bakterien mit unbeschädigter Membran kann nur das SYBR Green eindringen, daher erscheinen sie grün. Bei beschädigter Membran kommt auch das Propidiumiodid durch. Dieses weist eine rote Fluoreszenz auf.
(Foto: ETH Zürich, Lea Bircher)