Détail de l'archive
Pénétration des parfums dans l'organisme : un nouvel outil de quantification
14 mars 2019 |
De très nombreux produits d'usage courant contiennent des substances aromatiques et odorantes : cosmétiques, lessives et détergents, parfums d'ambiance, etc. Si ces composés ne sont pas ou pas totalement éliminés dans les stations d'épuration, ils se retrouvent tôt ou tard dans les lacs, les rivières et les eaux souterraines. Les fabricants qui désirent les utiliser sont donc contraints d'évaluer les risques qu'ils représentent pour l'environnement avant de pouvoir les intégrer à leurs produits. L'un des principaux paramètres à considérer est alors la capacité d'accumulation dans les poissons. Il se trouve cependant que ces substances sont très difficiles à tester : beaucoup se fixent facilement sur les matériaux et sont volatiles pour pouvoir être perçues par l'odorat. « En raison de ces propriétés, les molécules odorantes sont progressivement perdues au cours des tests », indique la biologiste Hannah Schug, qui prépare une thèse au département de Toxicologie de l'environnement sous la direction de Kristin Schirmer.
Une lignée de cellules intestinales utilisée comme barrière biologique
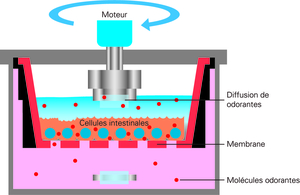
Pour pallier ces difficultés, Hannah Schug a travaillé à un nouveau dispositif pour évaluer les substances odorantes en collaboration avec l'un des principaux fabricants du marché. L'appareil, de la taille d'un petit Rubik's cube, est hermétique pour que les substances ne puissent pas se volatiliser et présente une surface intérieure absolument lisse, si bien que les composés qui y pénètrent ne peuvent pas adhérer à ses parois. L'intérieur du cube, appelé TransFEr, abrite deux compartiments séparés par une membrane constituée à partir d'une lignée de cellules intestinales reproduisant la paroi intestinale des poissons, voie privilégiée de pénétration de très nombreuses substances dans l'organisme. La substance à tester est introduite dans le compartiment supérieur ; il est ensuite possible de la doser dans le compartiment inférieur pour savoir combien de molécules ont traversé les cellules intestinales. Les valeurs obtenues indiquent l'intensité avec laquelle les poissons absorbent les substances testées par l'intestin et sont donc susceptibles de les accumuler dans leur organisme.
Une approche intéressante pour la recherche pharmaceutique
Au-delà de la toxicologie environnementale, l'appareil inventé par Hannah Schug pourrait être intéressant pour de nombreux domaines de recherche, comme la toxicologie humaine et la pharmacologie. Les sociétés pharmaceutiques utilisent déjà des lignées cellulaires humaines pour évaluer l'absorption des substances actives de médicaments à travers la paroi intestinale. Mais certaines de ces substances présentent des propriétés similaires à celles des parfums et sont donc difficiles à étudier. « Notre appareil permettrait maintenant de les tester », indique Schug. Et d'ajouter : « Une fois qu'il a été démontré qu'une substance était incapable de traverser les cellules intestinales humaines dans le système TransFEr, il devient inutile de la tester sur les animaux. » Il semble donc que, grâce à ce type d'essais sur cultures cellulaires, il soit bientôt possible de renoncer, au moins partiellement, à l'expérimentation animale en recherche environnementale et médicale.
La recherche d'alternatives à l'expérimentation animale
La recherche est encore tributaire de l'expérimentation animale pour déterminer la toxicité des substances chimiques et leur capacité d'accumulation dans les tissus. L'équipe de Kristin Schirmer recherche des alternatives à cette approche et travaille au développement d'outils techniques et méthodologiques permettant à l'avenir de réduire ou même d'éviter le recours aux essais sur les animaux.