Détail de l'archive
Constat de décès chez les bactéries
30 octobre 2018 |
La composition de la flore intestinale a une forte influence sur les défenses immunitaires et la nutrition de l'être humain. Il est par ailleurs apparu que la flore – ou le microbiote intestinal, comme l'appellent les spécialistes – se modifiait pendant l'évolution de beaucoup de maladies intestinales.
Actuellement, les possibilités d'utilisation thérapeutique des micro-organismes de l'intestin humain sont ainsi intensément étudiées, notamment à l'Institut de recherche sur l'alimentation, la nutrition et la santé (IFNH) de l'EPF de Zurich. Dans la thèse qu'elle vient de publier, la doctorante Lea Bircher s'est concentrée sur la conservation des entérobactéries. Pour que ces micro-organismes vivants puissent être utilisés en tant qu'auxiliaires thérapeutiques ou que compléments alimentaires, il importe en effet qu'ils traversent cette phase transitoire sans subir aucun dommage. La chercheuse a sélectionné six souches bactériennes remplissant différentes fonctions et a observé la façon dont elles supportaient trois mois de congélation à -80 °C ou de lyophilisation lorsque différents produits antigel leur étaient administrés.
Transfert de savoir méthodologique
Frederik Hammes, du département de microbiologie de l'environnement de l'Eawag a apporté son soutien au projet par son savoir-faire en matière de cytométrie en flux, une technique de mesure qui permet notamment des analyses beaucoup plus rapides que la culture de colonies en boîte de Pétri ou que les techniques de biologie moléculaire.
«La cytométrie en flux ne nous était pas totalement inconnue, signale Clarissa Schwab, qui a encadré la thèse de Lea Bircher à l'IFNH. Mais nous ne l'avions plus employée depuis des années dans notre laboratoire et nous avons donc été très heureux de pouvoir profiter de l'expérience de l'Eawag.»
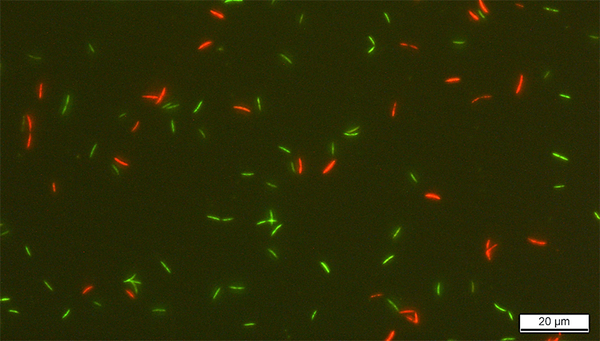
Frederik Hammes utilise cette technique depuis très longtemps pour analyser l'eau de boisson et les eaux usées et il dispose d'une grande expérience en matière de mise en évidence de la viabilité des bactéries vivant dans l'eau. Bircher et Hammes ont sélectionné ensemble la méthode la mieux adaptée pour évaluer l'état des bactéries intestinales après la conservation. Ils ont assez rapidement opté pour une coloration au SYBR green I et à l'iodure de propidium (SGPI) qui permet de reconnaître si la membrane des bactéries est intacte ou non. Les bactéries indemnes apparaissent en vert dans le cytomètre en flux tandis que les cellules endommagées sont colorées en rouge.
La raison de leur choix ? La grande expérience de l'Eawag avec la technique de marquage au SGPI : cette méthode a été optimisée pour la cytométrie en flux par l'équipe de Frederik Hammes et finalement standardisée en 2016. Son adéquation pour les entérobactéries sélectionnées par Bircher a été démontrée dans plusieurs essais menés dans le laboratoire de l'Eawag. Après une phase d'instruction à l'Eawag, la jeune chercheuse a pu réaliser ses propres analyses de cytométrie en flux dans les laboratoires de l'EPFZ.
Effet bénéfique des produits antigel
Afin d'évaluer le taux de survie des probiotiques à la conservation, Bircher a développé des cultures des différentes souches avant et après le traitement. La méthode au SGPI lui a livré des informations complémentaires précieuses sur la viabilité des différents échantillons. Elle a ainsi pu montrer dans son travail que l'ajout de substances antigel telles que le sucre, l'inuline ou le glycérol pouvait faire fortement augmenter le taux de survie des bactéries. L'efficacité de chacun de ces produits antigel variait cependant en fonction des micro-organismes et des techniques de conservation considérés.
Toutes les bactéries étudiées par Bircher suscitent de grands espoirs parmi les spécialistes ; elles sont considérées comme des «probiotiques de nouvelle génération». Mais de nombreux essais seront encore nécessaires avant qu'elles apparaissent réellement sur le marché.
Tout a débuté lors d'une conférence
L'idée d'une collaboration entre Clarissa Schwab et Frederik Hammes est née en 2015, lors d'une conférence de l'Eawag. Intitulé «How Dead Is Dead», ce colloque portait sur les limites de la vie bactérienne : à partir de quel moment une cellule bactérienne peut-elle être considérée comme morte et comment peut-on mettre cet état en évidence ? Les cellules bactériennes peuvent en effet entrer en dormance en ralentissant leurs processus métaboliques et physiologiques jusqu'à un niveau de non détectabilité. De telles cellules peuvent-elles être «réanimées» ? Ces questions continuent d'occuper les scientifiques – aussi bien dans le domaine médical que dans celui de l'eau potable.
Les travaux de Lea Bircher ont été financés par le Fonds national suisse (Sinergia 35150) et l'EPF de Zurich.
Publications
Photo
Bactéries intestinales de l'espèce Roseburia intestinalis colorées au SYBR green I et à l'iodure de propidium (SGPI). Seul le SYBR green I peut pénétrer dans les bactéries aux membranes intactes qui apparaissent donc en vert. Les membranes endommagées laissent également pénétrer l'iodure de propidium qui présente une fluorescence rouge.
(Photo : EPF Zurich, Lea Bircher)