Détail de l'archive
Recherches sur l'infiniment petit
19 juin 2018 |
Elles rendent les plastiques plus solides, filtrent les UV, neutralisent les odeurs de transpiration dans les T-shirts ou rendent les surfaces déperlantes : les nanoparticules synthétiques interviennent dans de nombreux produits. Elles mesurent entre un et cent nanomètres – le diamètre d'un cheveu est déjà de 10 000 nanomètres – et sont donc difficiles à appréhender, ce qui explique peut-être la méfiance du grand public à leur égard. Pourtant, les particules microscopiques ne sont en rien une invention exclusivement humaine. Les cendres volcaniques ou la fumée des feux de bois contiennent des nanoparticules naturelles ; de même, beaucoup de particules biologiques ou chimiques comme les gouttelettes de lipide dans le lait ou les petites protéines du sang sont de taille nanométrique.
Transformation dans les stations d'épuration
Les nanoparticules synthétiques peuvent être rejetées dans l'environnement – et ce, pendant tout le cycle de vie des produits. Quel est alors leur comportement et quels sont leurs effets ? Telles sont les questions qui occupent les chercheurs du monde entier depuis des années. L'un d'entre eux est Ralf Kägi, spécialiste des nanoparticules à l'Eawag. Dans une étude publiée en 2017, lui et son équipe ont étudié la transformation des nanoparticules d'oxyde de cuivre dans les eaux usées. Elles sont par exemple utilisées dans les pistes de conduction ou de commutation mais également dans l'imprégnation du bois. Les chercheurs estimaient que l'oxyde de cuivre pouvait se transformer en sulfure de cuivre dans les procédés d'épuration et perdre ainsi la plus grande partie de sa toxicité. Les résultats leur ont donné raison : les particules de cuivre se transforment en quelques minutes en covelline, un sulfure de cuivre que l'on trouve souvent dans la nature sous forme de fines couches sur d'autres roches. Selon Kägi, «les ions de cuivre originellement dissous se retrouvent liés et les particules perdent alors leurs propriétés de nanomatériau».
Beaucoup de nanoparticules se retrouvent dans les boues d'épuration
D'autres nanoparticules subissent également une transformation rapide dans les stations d'épuration et se retrouvent à 95-99% dans les boues. «Ces dernières sont incinérées et mises en décharge – les nanoparticules synthétiques sont ainsi retirées de la circulation», indique Kägi. Avec son équipe, il a réalisé plusieurs études sur les risques de différents nanomatériaux pour l'homme et l'environnement. «Nous avons commencé par le nanoargent qui est surtout utilisé dans les textiles. Puis nous avons effectués des essais en reproduisant les conditions naturelles dans des pilotes de l'Eawag avec des nanoparticules à base de cuivre, de zinc, de titane ou de cérium», raconte le chercheur. Le cérium est utilisé dans les poudres d'abrasion et les lentilles en verre, le titane dans les crèmes solaires et le cuivre dans les vernis à bateaux. Les résultats sont similaires pour tous les matériaux : «Les traitements d'épuration convertissent les nanoparticules actives en particules moins préoccupantes et les retirent ainsi très efficacement des eaux usées.»
Étude écotoxicologique des réactions d'ordre biologique
De son côté, le département de toxicologie de l'environnement s'intéresse plutôt aux mécanismes fondamentaux sous la direction de Kristin Schirmer. «Nous étudions notamment l'influence des nanoparticules métalliques les plus fréquentes sur les êtres vivants à différents niveaux d'organisation biologique et écologique : des algues aux biofilms, des lignées cellulaires et des embryons aux poissons», explique l'écotoxicologue Ahmed Tlili. Ces études sont menées au laboratoire où les concentrations utilisées sont en général plus élevées que dans la nature bien que de nombreux effets se manifestent à très faible concentration.
Les écotoxicologues ont ainsi étudié l'absorption des nanoparticules de cérium et d'oxyde de cérium par l'algue Chlamydomonas reinhardtii. Ces particules sont employées comme additifs, par exemple dans les inlays en céramique, les revêtements des fours autonettoyants ou les produits de polissage des verres spéciaux comme les pare-brises. Dans leur étude, les toxicologues ont comparé l'absorption des nanoparticules chez des algues de type sauvage et des algues mutantes sans paroi cellulaire. Ils n'ont observé aucune différence avec l'oxyde de cérium alors que le cérium dissous était plus facilement absorbé par les mutantes. Les scientifiques supposent que le cérium cellulaire se fixe à la paroi chez les algues non modifiées, ce qui l'empêche de la traverser.
«Les algues sont souvent dans l'incapacité d'absorber les nanoparticules, confirme Ahmed Tlili. Toutefois, si des constituants métalliques se dissolvent dans l'eau, ils peuvent avoir des effets sur les algues et les bactéries. Il s'agit alors d'effets indirects des nanoparticules.» Les biofilms, en revanche, réagissent directement aux particules : «La croissance et le taux de respiration baissent chez les organismes microbiologiques. Les organismes de niveau supérieur disposent alors de moins de nourriture», explique Tlili.
La distinction entre sources naturelles et origine artificielle
Grâce à la pluralité des recherches déjà effectuées, on sait mieux aujourd'hui comment les nanoparticules les plus courantes sont rejetées dans l'environnement et où elles finissent par aboutir. De même, de nombreuses méthodes d'analyse sont aujourd'hui disponibles. Elles permettent par exemple de savoir si les nanoparticules sont d'origine naturelle ou synthétique. C'est par exemple le cas du dioxyde de titane. Utilisé dans les crèmes solaires, il se dissout en partie dans l'eau lors de la baignade. Les piscines couvertes peuvent l'éliminer grâce à leurs filtres mais les piscines ouvertes, les lacs et des rivières ne disposent pas de telles barrières. D'un autre côté, le dioxyde de titane existe aussi à l'état naturel : dans le milieu aquatique sa concentration est de l'ordre de 5000 particules par millilitre.
Dans une étude publiée récemment, des chercheurs de l'université de Vienne, de l'Eawag et de l'école supérieure suédoise d'agriculture ont étudié la part du dioxyde de titane des crèmes solaires présente dans les lacs et rivières et se déposant ensuite dans le sédiment. Ils se sont basés sur le fait que les particules naturelles de titane s'accompagnent souvent de fer, de manganèse, de plomb ou d'aluminium alors que les nanoparticules de synthèse ne présentent pas de «bruit de fond» typique. «Nous pouvons ainsi reconnaître d'où viennent les particules», commente Kägi. Les chercheurs ont constaté que les concentrations de dioxyde de titane augmentaient au cours de l'été dans le Danube. Cet apport à travers les crèmes solaires était cependant très faible comparé aux teneurs naturelles. Aujourd'hui, une telle distinction est également possible pour l'oxyde de cérium. Kägi explique le principe utilisé : «Contrairement à son homologue synthétique, l'oxyde de cérium naturel est généralement accompagné de lanthane. C'est ce qui nous permet de le reconnaître.»
Pas de toxicité aiguë en conditions naturelles
Des experts venus de tous les pays se sont réunis en mars 2017 au Monte Verità sous la houlette de l'Empa et de l'Eawag pour faire le point sur les progrès réalisés ces dix dernières années dans la recherche sur les nanomatériaux et discuter des pistes à suivre. Ils ont retenu que des effets pouvaient être observés au laboratoire chez divers organismes après une période assez courte d'exposition aux nanoparticules. Ces effets se manifestent cependant surtout à des concentrations élevées ne survenant jamais dans l'environnement. «Ces essais de laboratoire sont importants pour mieux comprendre les phénomènes mais ils sont souvent assez éloignés de la réalité, indique Kägi. En conditions réalistes, nous n'observons pas d'effets aigus sur les organismes ou les écosystèmes – à moins, bien sûr, que les nanomatériaux ne soient constitués d'éléments toxiques comme les métaux lourds.»
De nouvelles priorités pour la recherche
Les scientifiques de l'Eawag souhaitent maintenant se concentrer sur les nombreuses questions encore sans réponse : Quels peuvent être les effets d'une exposition chronique aux nanoparticules synthétiques ? Comment les communautés biotiques et les écosystèmes réagissent-ils s'ils sont exposés de façon chronique à un cocktail de nanomatériaux ? Qu'advient-il des nanomatériaux lorsqu'ils sont incinérés ? «Nous voulons profiter de la grande quantité de données disponibles pour améliorer la modélisation des risques, ajoute Tlili. Par ailleurs, nous allons moins nous concentrer sur les nanomatériaux natifs pour nous intéresser aux particules une fois qu'elles ont vieilli dans l'environnement.» Ce dernier aspect préoccupe également l'équipe de Kägi. Les chercheurs ont en effet prévu d'étudier la transformation des nanoparticules de dioxyde de cérium pendant l'épuration des eaux puis le traitement et l'incinération des boues. Ils souhaitent également savoir si les nanoparticules peuvent être remobilisées à partir des cendres obtenues avec les boues d'épuration.
Publications
Nowack, B., 2009. The behavior and effects of nanoparticles in the environment. Environ. Pollut. 157, 1063–1064.
Photos
L'écotoxicologue Xiaomei Li montrant des nanoparticules absorbées par des cellules.
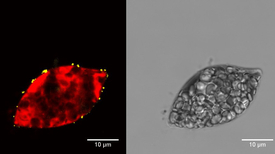
Vues de l'algue Euglena gracilis après deux heures d'exposition à des nanoparticules fluorescentes. Des particules fluorescentes (gauche, jaune) se trouvent à l'extérieur de la cellule d'algues, dont l'intérieur est rouge fluorescent (par rapport à l'aspect en microscopie à transmission à droite). (Source: Eawag, Xiaomei Li)

À l'Eawag, les scientifiques testent différentes méthodes pour l'analyse des nanoparticules de dioxyde de titane libérées dans l'eau par les crèmes solaires lors de la baignade.

Après la baignade, les chercheurs prélèvent des échantillons d'eau afin de rechercher les nanoparticules synthétiques de dioxyde de titane provenant de la crème solaire.

